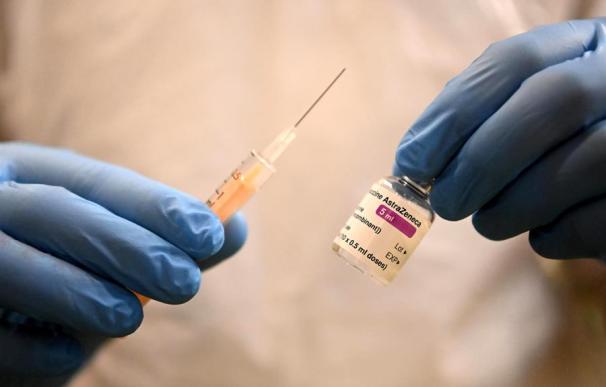
No hay acuerdo. La Comisión Europea ha pedido este miércoles a los Veintisiete que busquen una posición "lo más coordinada posible" sobre AstraZeneca, en una reunión en la que los ministros de Salud del bloque expusieron diferentes interpretaciones y pidieron más estudios sobre el impacto de la vacuna. "Los Estados miembro de la UE compartieron diferentes interpretaciones sobre las conclusiones" de la Agencia Europea del Medicamento (EMA) sobre AstraZeneca, informó en un comunicado la presidencia portuguesa de la UE, que convocó una reunión extraordinaria de los titulares de Salud.
Tanto la Comisión Europea como Portugal apelaron a los Veintisiete a encontrar una posición común en la reunión, realizada por videoconferencia, en la que sí hubo consenso sobre la necesidad de realizar más estudios sobre el impacto de la vacuna en "grupos específicos".
Durante la reunión por videoconferencia que los responsables de Salud han mantenido con carácter de urgencia, la comisaria Stella Kyriakides ha pedido a los gobiernos del bloque que "hablen con una sola voz" para "mejorar la confianza pública en las vacunas". "La experiencia de AstraZeneca demuestra que nuestro sistema de farmacovigilancia funciona. Pero es esencial que sigamos un enfoque coordinado en la UE", ha instado la chipriota.
Marta Temido, ministra de Sanidad de Portugal, país que este semestre ostenta la presidencia de turno de la UE, se ha pronunciado en una línea similar y ha pedido a los Estados miembros que "trabajen para tener una posición lo más coordinada posible", según ha informado en un comunicado. "Esta es una decisión técnica, no política. Debemos continuar siguiendo la mejor información científica que da la EMA en sus opiniones. No debemos olvidar que las decisiones individuales afectan a todos", ha dicho.
Durante la reunión telemática, los Estados miembros compartieron sus "diferentes interpretaciones" sobre las conclusiones de la EMA en relación al suero de AstraZeneca y pidieron al organismo sanitario europeo más información farmacológica sobre la vacuna para "grupos específicos" de la población.
Sin embargo, algunos países han anunciado tras conocer las conclusiones de la EMA distintos enfoques sobre la administración de la vacuna de AstraZeneca. Bélgica, por ejemplo, sólo la administrará a mayores de 55 años, mientras que Alemania, Países Bajos o Estonia, han elevado el umbral hasta los 60 años.
En España, el Ministerio de Sanidad ha propuesto a las comunidades autónomas, en el seno del pleno del Consejo Interterritorial del Sistema Nacional de Salud (CISNS), administrar la vacuna contra el coronavirus desarrollada por AstraZeneca sólo a las personas mayores de 60 años.
Horas antes, el comité de seguridad de la EMA ha concluido que existe una "posible relación" entre la vacuna de AstraZeneca contra el coronavirus y los coágulos sanguíneos con niveles bajos de plaquetas. Por ello, el organismo sanitario de la UE ha establecido que estos acontecimientos adversos deben figurar en la lista de efectos secundarios "muy raros" de la vacuna. No obstante, ha recalcado que los beneficios de la vacuna siguen superando los posibles riesgos.
"Cualquier decisión tendrá en cuenta la situación global"
De esta forma, la EMA ha dejado a los países la responsabilidad de restringir o no su uso en determinados grupos de edad. "Cualquier decisión nacional sobre el uso óptimo en las campañas de vacunación también tendrá en cuenta la situación de la pandemia en cualquier país individual, y otros factores como la hospitalización y la disponibilidad de vacunas", ha apuntado la directora ejecutiva de la EMA, Emer Cooke, en la rueda de prensa en la que ha explicado las conclusiones de la institución.
Cooke ha anunciado que, no obstante, el comité de seguridad de la EMA (PRAC, por sus siglas en inglés) ha solicitado "nuevos estudios y modificaciones de los que están en curso para proporcionar más información y tomará cualquier otra medida necesaria". De la misma forma, se va a exigir a AstraZeneca que analice a fondo estas trombosis a través de ensayos clínicos.


Hemos bloqueado los comentarios de este contenido. Sólo se mostrarán los mensajes moderados hasta ahora, pero no se podrán redactar nuevos comentarios.
Consulta los casos en los que lainformacion.com restringirá la posibilidad de dejar comentarios