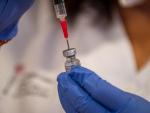
La comisaria de Salud, Stella Kyriakides, ha afirmado que todas las fórmulas son analizadas con evidencias y datos científicos, por lo que Sputnik V necesitaría el mismo nivel requerido de eficacia y seguridad.

La comisaria de Salud, Stella Kyriakides, ha afirmado que todas las fórmulas son analizadas con evidencias y datos científicos, por lo que Sputnik V necesitaría el mismo nivel requerido de eficacia y seguridad.

La recién nombrada ministra de Sanidad ha hecho su primera intervención en el Congreso de los Diputados sobre la posibilidad de obtener la 'Sputnik V'.

Sanidad se desmarcaría del planteamiento de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés), quien optó por aprobarla para todos los ciudadanos.

Ese suministro forma parte del segundo pedido de la UE, de 200 millones de dosis, y llega tras el 'rifirrafe' de las altas instituciones europeas con AstraZeneca.

"Paso adelante en vacunas", ha anunciado la presidenta de la Comisión Europea a través de las redes sociales. La cifra se añade a las 40 millones de unidades que iba a entregar la empresa en este trimestre.

Bruselas, que temía que la farmacéutica estuviese entregando al Reino Unido dosis que correspondían a los Veintisiete, quiere controlar cuántas vacunas se producen en su territorio y a qué países se destinan.

Los resultados combinados de 4 ensayos clínicos en el Reino Unido, Brasil y Sudáfrica mostraron que la vacuna era segura y eficaz para prevenir la Covid-19 en personas a partir de los 18 años.

La publicación llega después de que Charles Michel amenazara con activar el artículo 122 del Tratado de Funcionamiento de la UE, con el que se podría requisar la producción y tomar el control de las plantas.
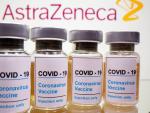
El acuerdo con Reino Unido dejó sin margen a la farmacéutica, que se siente comprometida por haberlo firmado tres meses antes que con Bruselas y en el que se incluiría que la producción británica iría a las islas.

La directora de la EMA, Emer Cooke, aseguró que los ensayos que han sido remitidos a la institución sobre la efectividad de las dosis incluyen una cantidad "muy pequeña" de población mayor.

En vísperas de que la Agencia Europea del Medicamento apruebe la vacuna de la farmacéutica continúa el pulso comercial. Bruselas mantiene su objetivo de vacunar al 70% de la población antes del verano

Londres tiene asegurado el suministro para lo que queda de año, mientras que la UE ven cómo Pfizer y Moderna se retrasan en la entrega.

El virólogo español, Mariano Esteban, el encargado de desarrollar la dosis española más avanzada por su eficacia del 100% en ratones
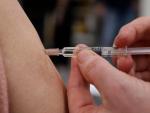
Bruselas ha desvelado la negativa de la compañía a acudir a esta cita tras la polémica por la reducción de las dosis que llegarán a los países europeos. Europa aún estudia posibles acciones legales.

Según Ursula von der Leyen, se tratará de un mecanismo permanente para asegurar "financiación que se pueda prever a largo plazo" y reunirá a "empresas tecnológicas de vanguardia, productores y reguladores".

"Todo indica que es una inyección que podría ser utilizada esta misma semana en el ámbito europeo", ha explicado el aún ministro de Sanidad.

El magistrado destaca que la mujer se vacuna contra la gripe todos los años y añade que los informes de la residencia y del forense coinciden en que la vacunación atiende a la protección de la implicada.
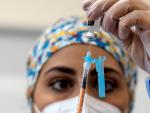
Los nuevos virales comenzarán a administrarse en paralelo a la de la farmacéutica estadounidense, que se lleva utilizando en nuestro país desde el 27 de diciembre.
La Agencia Europea del Medicamento ha evaluado datos sobre estudios de laboratorio, información sobre la calidad de la vacuna (sus ingredientes y el proceso de producción) y evidencia sobre su seguridad.

La reciente aprobación de la Agencia Europea del Medicamento urge al Ministerio de Sanidad y las CCAA a agilizar el suministro de dosis de Pfizer, de cuya partida total se ha administrado menos del 20%.

El visto bueno de los científicos del regulador europeo a la candidata de la farmacéutica estadounidense allana el camino para la recepción de 8.348.979 dosis iniciales en España.

Como todos los medicamentos, la vacuna puede desencadenar reacciones adversas leves (fiebre o dolor en el lugar de la inyección) o, con menor frecuencia, otras más graves (encefalitis, vasculitis, neuralgia, etc).

El Ejecutivo comunitario, que negocia la compra conjunta de vacunas para los Estados miembros de la UE, se ha dotado de una cartera diversificada de contratos con diferentes desarrolladores de Europa y EEUU.

El Ejecutivo comunitario, que negocia la compra conjunta de vacunas para los Estados miembros de la UE, se ha dotado de una cartera diversificada de contratos con diferentes desarrolladores de Europa y EEUU.

El organismo que lidera Úrsula von der Leyen ha firmado la licencia de comercialización condicional del antídoto "al mismo tiempo y en las mismas condiciones" en todos los Estados miembros.
Página 1 de 10